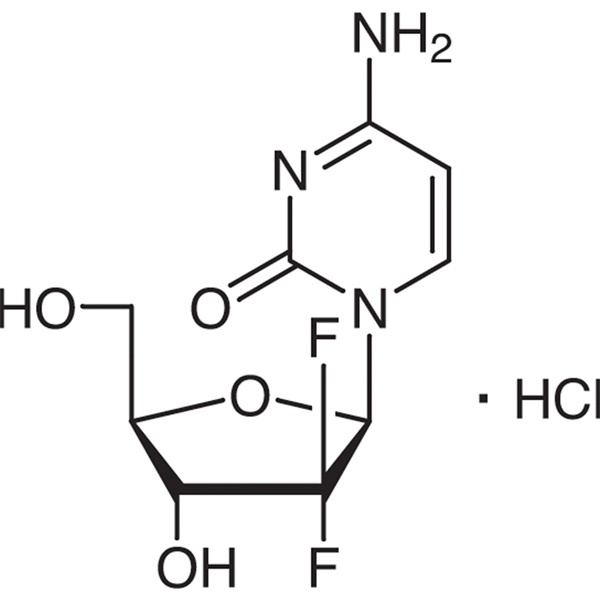
Gemcitabine Hydrochloride CAS 122111-03-9 API USP35 Standartı
Ruifu Chemical yüksək keyfiyyətli, kommersiya istehsalı ilə Gemcitabine Hydrochloride (CAS: 122111-03-9) aparıcı istehsalçısıdır.Ruifu Chemical dünya miqyasında çatdırılma, rəqabətqabiliyyətli qiymət, əla xidmət, kiçik və toplu miqdarları təmin edə bilər.Gemcitabine Hydrochloride satın alın,Please contact: alvin@ruifuchem.com
| Kimyəvi adı | Gemsitabin hidroxlorid |
| Sinonimlər | Gemsitabin HCl;2'-Deoksi-2',2'-Difluorositidin hidroklorid;dFdC;dFdCyd;Gemzar;LY188011 Hidroklorid;Gemcitera;Gemsar |
| CAS nömrəsi | 122111-03-9 |
| Əlaqədar CAS | 95058-81-4 - Pulsuz baza |
| Səhm Vəziyyəti | Stokda, İstehsal Gücü 5 Ton |
| Molekulyar Formula | C9H12ClF2N3O4 |
| Molekulyar çəki | 299.66 |
| Ərimə nöqtəsi | >250 ℃ |
| Çatdırılma Vəziyyəti | Ətraf mühitin temperaturu altında |
| COA və MSDS | Mövcuddur |
| Mənşə | Şanxay, Çin |
| Brend | Ruifu Kimya |
| Maddə | Spesifikasiyalar | Nəticələr |
| Görünüş | Ağ kristal toz, qoxusuz | Uyğundur |
| Həlledicilik | Suda həll olur, metanolda az həll olur, asetonda praktiki olaraq həll olunmur | Uyğundur |
| İdentifikasiya IR | IR spektri uyğun olmalıdır istinad standartı | Uyğundur |
| İdentifikasiya xlorid | Müsbət.Xlorid üçün testlərin tələblərinə cavab verir | Uyğundur |
| Həllin görünüşü | Həll S aydın və daha sıx deyil BY7 referans məhlulundan daha rənglidir | Uyğundur |
| pH | 2.0~3.0 | 2.6 |
| Xüsusi Fırlanma [α]20/D | +43,0°-dən +50,0°-ə qədər | +47,5° |
| Ağır metallar (Pb) | ≤10ppm | <10ppm |
| Qurutma zamanı itki | ≤1,00% | 0,3% |
| Alovlanma zamanı qalıq | ≤0,10% | 0,03% |
| Əlaqədar Maddələr | ||
| sitozin | ≤0,10% | 0,01% |
| α-izomer | ≤0,10% | 0,01% |
| Hər hansı digər murdarlıq | ≤0,10% | 0,04% |
| Ümumi çirkləri | ≤0,20% | 0,1% |
| Qalıq həlledicilər | ||
| Metanol | ≤0,30% | Aşkarlanmadı |
| Toluol | ≤0,01% | Aşkarlanmadı |
| Dixlorometan | ≤0,01% | Aşkarlanmadı |
| Aseton | ≤0,50% | 0,1% |
| Təhlil | 97.5% ~ 101.5% (Qurudulmuş əsasda hesablanır) | 99,9% |
| Nəticə | USP35 Standartına uyğundur | |
Paket:Şüşə, alüminium folqa çanta, 25 kq/Karton baraban və ya müştərinin tələbinə uyğun olaraq.
Saxlama Vəziyyəti:Konteyneri sıx bağlı saxlayın və sərin, quru və yaxşı havalandırılan anbarda uyğun olmayan maddələrdən uzaq saxlayın.Birbaşa günəş işığına, nəmə və həddindən artıq istiyə məruz qalmaqdan çəkinin.
Göndərmə:FedEx / DHL Express ilə hava ilə bütün dünyaya çatdırın.Sürətli və etibarlı çatdırılma təmin edin.


Risk kodları R21 - Dəri ilə təmasda zərərlidir
R36/38 - Gözləri və dərini qıcıqlandırır.
R46 - İrsi genetik ziyana səbəb ola bilər
R62 - Mümkün məhsuldarlığın pozulması riski
R63 - doğmamış uşağa mümkün zərər riski
Təhlükəsizlik Təsviri S25 - Gözlərlə təmasdan çəkinin.
S26 - Gözlərlə təmasda olduqda, dərhal bol su ilə yuyun və həkimə müraciət edin.
S36/37 - Müvafiq qoruyucu geyim və əlcəklər geyin.
S53 - Ekspozisiyadan çəkinin - istifadə etməzdən əvvəl xüsusi təlimatları əldə edin.
WGK Almaniya 3
RTECS HA3840000
HS Kodu 2942000000
Gemcitabine Hydrochloride (CAS: 122111-03-9) anti-metabolik və antineoplastik olan sintetik yeni difluoronükleozid dərmanıdır.O, Eli Lilly və Şirkəti tərəfindən tədqiq edilmiş və hazırlanmışdır və 1995-ci ildə Cənubi Afrika, İsveç, Hollandiya, Avstraliya və digər ölkələrdə siyahıya alınması üçün təsdiq edilmişdir. Amerika Birləşmiş Ştatlarının Qida və Dərman İdarəsi (FDA) onu birinci dərəcəli terapiya kimi təsdiq etmişdir. kiçik hüceyrəli olmayan ağciyər xərçəngi və pankreas xərçənginin klinik müalicəsi üçün.
Son illərdə Gemcitabine, Paclitaxel, Docetaxel, Vinorebine kimi yeni dərmanlar kiçik hüceyrəli olmayan ağciyər xərçənginin (qısaldılmış NSCLC) müalicəsi üçün təsirli dərmanlardır.Ənənəvi kimyaterapiya dərmanları ilə müqayisədə bu dərmanlar yüksək müalicəvi təsir və aşağı toksiklik üstünlüklərinə malikdir.Gemcitabine Hydrochloride yeni nəsil anti-metabolit dərmanıdır və hüceyrə dövrü üçün xüsusi dərman növüdür, DNT sintezi mərhələsində, yəni hüceyrələrin S fazasında böyük rol oynayır.Müəyyən şərtlərdə bu dərman hüceyrələrin G1 fazasından S fazasına keçməsinin qarşısını ala bilər və kiçik hüceyrəli olmayan ağciyər xərçəngi (KHDAK) üçün güclü anti-xərçəng fəaliyyətinə malikdir.Xarici tədqiqatlar göstərmişdir ki, QHDAK üçün yalnız Qemsitabin hidroxlorid ilə birdəfəlik müalicənin effektivliyi təxminən 18% ~ 35%, sisplatinlə kombinə edilmiş müalicə isə QHDAK üçün effektivliyin 41,7% təşkil edir.Qabaqcıl NSCLC-də karboplatinin effektiv dərəcəsi 16% təşkil edir ki, bu da sisplatinə bənzəyir, lakin xüsusilə mədə-bağırsaq reaksiyaları, sümük iliyinin yatırılması və böyrək və sinir sonlarının toksik reaksiyası üçün aşağı toksikliyə malikdir.Karboplatinlə birlikdə onların hər ikisi qarşılıqlı koordinasiyaya və əlavə təsirə malikdir və daha yüksək müalicəvi təsir göstərə bilər.
Gemsitabin hidroxlorid
C9H11F2N3O4·HCl 299,66
Sitidin, 2′-deoksi-2′,2′-difluro-, monohidroxlorid.
2′-Deoksi-2′,2′-difluorositidin monohidroklorid (β-izomer) [122111-03-9].
» Gemcitabine Hydrochloride, olduğu kimi hesablanmış 97,5 faizdən az və 101,5 faizdən çox olmayan C9H11F2N3O4·HCl ehtiva edir.
[Diqqət - Gemcitabine Hydrochloride güclü sitotoksik agentdir.Hissəciklərin tənəffüs edilməsinin və dərinin ona məruz qalmasının qarşısını almaq üçün çox diqqətli olmaq lazımdır.]
Qablaşdırma və saxlama - Sıx qablarda saxlayın.
Etiketləmə - Enjekte edilə bilən dozaj formalarının hazırlanmasında istifadə üçün nəzərdə tutulduqda, etiket onun steril olduğunu və ya inyeksiya edilə bilən dozaj formalarının hazırlanması zamanı əlavə emal edilməli olduğunu bildirir.
USP Referans standartları <11>-
USP Sitozin RS
USP Endotoksin RS
USP Gemcitabine Hydrochloride RS
Şəxsiyyət -
A: İnfraqırmızı udma <197K>.
B: Xlorid <191> üçün sınaqların tələblərinə cavab verir.
Xüsusi fırlanma <781S>: +43 ilə +50 arasında, 20-də.
Test məhlulu: ml başına 10 mq.
pH <791>: 2,0 ilə 3,0 arasında, hər ml başına 10 mq olan məhlulda.
Alışma zamanı qalıq <281>: 0,1%-dən çox olmamalıdır.
Ağır metallar, Metod I <231>: 0,001%.
Xromatoqrafik təmizlik-
Həll A- Təhlildə Mobil mərhələ üçün göstərişlərə uyğun olaraq davam edin.
Həll B-Süzülən və qazı alınmış metanol hazırlayın.
Mobil faza-Xromatoqrafik sistemə uyğun olaraq A məhlulunun və B məhlulunun dəyişkən qarışıqlarından istifadə edin.Lazım gələrsə, düzəlişlər edin (Xromatoqrafiya 621-də Sistem Uyğunluğuna baxın).
Sistem uyğunluğu həlli - Təhlildə göstərildiyi kimi davam edin.
Standart məhlul-Dəqiq çəkilmiş miqdarda USP Gemcitabine Hydrochloride RS və USP Cytosine RS-ni suda həll edin və kəmiyyətcə və lazım gələrsə, hər bir ml üçün təxminən 2 µg məlum konsentrasiyaya malik məhlul əldə etmək üçün mərhələli şəkildə seyreltin.
Sınaq məhlulu - Dəqiq çəkilmiş təxminən 50 mq Gemsitabin hidroxloridini 25 ml-lik ölçülü kolbaya köçürün, içində həll edin və su ilə həcminə qədər seyreltin və qarışdırın.
Xromatoqrafik sistem (bax. Xromatoqrafiya 621) - Təhlil altında göstərildiyi kimi hərəkət edin.Xromatoqraf aşağıdakı kimi proqramlaşdırılır.
Vaxt (dəqiqə) A məhlulu (%) Məhlul B (%) Elüsyon
0–8 97 3 izokratik
8–13 97®50 3®50 xətti qradiyent
13–20 50 50 izokratik
20–25 50®97 50®3 yenidən tarazlıq
Sistem uyğunluğu məhlulunun xromatoqrafını aparın və Prosedur üçün göstərildiyi kimi pik cavabları qeyd edin: nisbi saxlama müddətləri gemsitabin-anomer üçün təxminən 0,5 və gemsitabin üçün 1,0-dır;gemsitabin-anomer və gemsitabin arasındakı rezolyutsiya, R, 8.0-dən az deyil;və gemsitabin üçün tullantı əmsalı 1,5-dən çox deyil.Standart məhlulun xromatoqrafını aparın və Prosedur üçün göstərildiyi kimi pik reaksiyaları qeyd edin: nisbi saxlama müddətləri sitozin üçün təxminən 0,1 və gemsitabin üçün 1,0-dır;təkrar inyeksiyalar üçün nisbi standart sapma 2,0%-dən çox deyil.
Prosedur-Xromatoqrafa Standart məhlul və Test məhlulunun bir həcmini (təxminən 20 µL) ayrıca yeridin, xromatoqramı qeyd edin və bütün pik reaksiyalarını ölçün.Gemsitabinin qəbul etdiyi hissədə sitozinin faizini düsturla hesablayın:
2.5(Cc / W)(rt / rs)
burada Cc standart məhlulda USP Cytosine RS konsentrasiyasıdır, hər ml üçün µg ilə;W qəbul edilən Gemsitabinin mq ilə çəkisidir;rt Test məhlulunda sitozin üçün pik cavabdır;və rs Standart məhlulda sitozin üçün cavabdır: 0,1%-dən çox olmayan sitozinə rast gəlinir.Gemsitabinin qəbul edilən hissəsində sitozindən başqa hər bir çirkin faizini düsturla hesablayın:
2.5(Cs / W)(ri / rs)
burada Cs Standart məhlulda USP Gemcitabine Hydrochloride RS konsentrasiyasıdır, hər ml üçün µg ilə;W qəbul edilən Gemsitabinin mq ilə çəkisidir;ri Test məhlulunda hər bir çirk üçün pik cavabdır;və rs Standart məhlulda gemsitabinə görə cavabdır: 0,1%-dən çox olmayan gemsitabin-anomer və ya hər hansı digər fərdi çirk tapılmamışdır;və bütün çirklərin cəmi 0,2%-dən çox deyil.Bütün çirklərin cəmindən kəmiyyət həddindən (0,02%) aşağı olan zirvələri çıxarın.
Digər tələblər-Etiketdə Gemcitabine Hydrochloride-in steril olduğu qeyd edilərsə, o, Bakterial endotoksinlər və İnyeksiya üçün Gemsitabin altında sterillik tələblərinə cavab verir.Etiketdə Gemcitabine Hydrochloride inyeksiya edilə bilən dozaj formalarının hazırlanması zamanı əlavə emal edilməli olduğu qeyd edilərsə, o, Gemcitabine for Injection altında Bakterial endotoksinlərə dair tələblərə cavab verir.
Təhlil-
Mobil faza - 1000 ml suda 13,8 q monobazlı natrium fosfat və 2,5 mL fosfor turşusu olan süzülmüş və qazsız məhlul hazırlayın.[qeyd-Bu məhlulun pH-ı 2,4 ilə 2,6 arasındadır.]
Sistem uyğunluğu üçün həll - Təxminən 10 mq Gemsitabin hidroxloridini kiçik flakona köçürün, hər ml metanol üçün 168 mq kalium hidroksid olan 4 mL məhlul əlavə edin, qapağı möhkəm bağlayın və sonikləşdirin.6-16 saat ərzində 55 dərəcə qızdırın, soyumağa icazə verin və içindəkiləri ardıcıl olaraq 1% (v/v) fosfor turşusu ilə yuyulmaqla 100 ml-lik ölçülü kolbaya köçürün.Həcmi 1% fosfor turşusu ilə seyreltin və qarışdırın.[Qeyd-Bu məhlulda hər ml gemsitabin α-anomerinə təxminən 0,02 mq daxildir.]
Standart preparat - Dəqiq çəkilmiş miqdarda USP Gemcitabine Hydrochloride RS-ni suda həll edin və kəmiyyətcə və lazım gələrsə, hər ml üçün təxminən 0,1 mq məlum konsentrasiyaya malik məhlul əldə etmək üçün su ilə mərhələli şəkildə seyreltin.
Təhlilin hazırlanması - Dəqiq çəkilmiş təxminən 20 mq Gemsitabin hidroxloridini 200 ml-lik ölçülü kolbaya köçürün, orada həll edin və su ilə həcminə qədər seyreltin və qarışdırın.
Xromatoqrafik sistem (bax: Xromatoqrafiya <621>)-Maye xromatoqraf 275 nm detektor və 5 µm qablaşdırma L7 ehtiva edən 4,6 mm × 25 sm sütunla təchiz edilmişdir.Axın sürəti dəqiqədə təxminən 1,2 ml-dir.Sistem uyğunluğu məhlulunun xromatoqrafını aparın və Prosedur üçün göstərildiyi kimi pik reaksiyaları qeyd edin: gemsitabin-anomer və gemsitabin arasındakı rezolyutsiya, R, 8.0-dən az deyil;və gemsitabindən müəyyən edilən tullantı əmsalı 1,5-dən çox deyil.Standart preparatı xromatoqraf edin və Prosedur üçün göstərildiyi kimi pik reaksiyaları qeyd edin: təkrar inyeksiyalar üçün nisbi standart kənarlaşma 1,0%-dən çox deyil.
Prosedur-Xromatoqrafa Standart preparat və Təhlil preparatının bərabər həcmlərini (təxminən 20 µL) ayrı-ayrılıqda yeridin, xromatoqramları qeyd edin və əsas zirvələr üçün cavabları ölçün.C9H11F2N3O4·HCl-in mq ilə miqdarını düsturla qəbul edilən Qemsitabin hidroxlorid hissəsində hesablayın:
200C(rU / rS)
burada C Standart preparatda USP Gemcitabine Hydrochloride RS-in mL başına mq ilə konsentrasiyasıdır;və rU və rS müvafiq olaraq Analiz hazırlığından və Standart preparatdan əldə edilən pik cavablardır.
-

Gemcitabine Hydrochloride CAS 122111-03-9 API U...
-

Gemcitabine CAS 95058-81-4 Təhlil 98.0~102.0%
-

Cefotiam Hydrochloride CAS 66309-69-1 API USP S...
-

Doxorubicin Hydrochloride CAS 25316-40-9 API ABŞ...
-

Enalapril Maleat CAS 76095-16-4 Təhlil 98.0~102...
-

Guanfacine Hidroklorid Guanfacine HCl CAS 291...
-

İrinotekan Hidroklorid CAS 100286-90-6 Saflıq...
-

Levetiracetam LEV CAS 102767-28-2 API Fabrika Ü...
-

Naltrekson Hidroklorid CAS 16676-29-2 API USP...
-

Noskapin Hidroklorid Hidrat CAS 912-60-7 AP...
-

Levodopa (L-DOPA) CAS 59-92-7 99.0~100.5% USP B...
-

Darunavir CAS 206361-99-1 Anti-HİV Saflığı ≥99.0...
-

Ezetimibe CAS 163222-33-1 Təmizlik 98,5% ~ 102,0% (...
-

Lasofoksifen Tartrat CAS 190791-29-8 Chiral Pu...
-

Bortezomib CAS 179324-69-7 Saflıq ≥99.0% (HPLC)...
-

CAS 274901-16-5 Saflıq ≥99.0% (HPLC) API