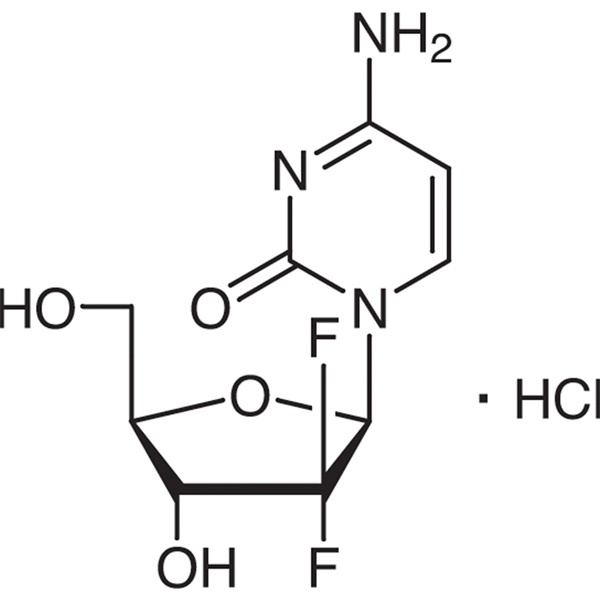
Гемцытабін гідрахларыд CAS 122111-03-9 Стандарт API USP35
Ruifu Chemical з'яўляецца вядучым вытворцам гемцытабіну гідрахларыду (CAS: 122111-03-9) з высокай якасцю камерцыйнай вытворчасці.Ruifu Chemical можа забяспечыць дастаўку па ўсім свеце, канкурэнтаздольную цану, выдатны сэрвіс, невялікія і оптавыя аб'ёмы.Купля гемцитабина гідрахларыд,Please contact: alvin@ruifuchem.com
| Хімічная назва | Гемцитабина гідрахларыд |
| Сінонімы | Гемцитабин HCl;2'-дезокси-2',2'-дифторцитидина гідрахларыд;dFdC;dFdCyd;Гемзар;LY188011 гідрахларыд;Гемцытэра;Гемсар |
| Нумар CAS | 122111-03-9 |
| Звязаны CAS | 95058-81-4 - Бясплатная база |
| Стан запасаў | У наяўнасці, вытворчая магутнасць 5 тон |
| Малекулярная формула | C9H12ClF2N3O4 |
| Малекулярная маса | 299,66 |
| Тэмпература плаўлення | >250 ℃ |
| Умова дастаўкі | Пры тэмпературы навакольнага асяроддзя |
| COA і MSDS | Даступны |
| Паходжанне | Шанхай, Кітай |
| Марка | Ruifu Chemical |
| Пункт | Тэхнічныя характарыстыкі | Вынікі |
| Знешні выгляд | Белы крышталічны парашок без паху | Адпавядае |
| Растваральнасць | Раствараецца ў вадзе, слаба раствараецца ў метаноле, практычна не раствараецца ў ацэтоне | Адпавядае |
| Ідэнтыфікацыя ВК | ІЧ-спектр павінен адпавядаць эталоннага стандарту | Адпавядае |
| Ідэнтыфікацыя Хларыд | Пазітыўны.Ён адпавядае патрабаванням выпрабаванняў на хларыд | Адпавядае |
| Знешні выгляд раствора | Раствор S празрысты і не больш інтэнсіўна каляровы, чым эталонны раствор BY7 | Адпавядае |
| pH | 2,0~3,0 | 2.6 |
| Удзельнае кручэнне [α]20/D | ад +43,0° да +50,0° | +47,5° |
| Цяжкія металы (Pb) | ≤10 частак на мільён | <10 частак на мільён |
| Страты пры сушцы | ≤1,00% | 0,3% |
| Рэшткі пры гарэнні | ≤0,10% | 0,03% |
| Роднасныя рэчывы | ||
| Цытазін | ≤0,10% | 0,01% |
| α-Ізамер | ≤0,10% | 0,01% |
| Любыя іншыя прымешкі | ≤0,10% | 0,04% |
| Агульныя прымешкі | ≤0,20% | 0,1% |
| Рэшткавыя растваральнікі | ||
| Метанол | ≤0,30% | Не выяўлена |
| Талуол | ≤0,01% | Не выяўлена |
| Дыхлорметан | ≤0,01% | Не выяўлена |
| ацэтон | ≤0,50% | 0,1% |
| аналіз | 97,5%~101,5% (у разліку на сухую аснову) | 99,9% |
| Заключэнне | Адпавядае стандарту USP35 | |
пакет:Бутэлька, мяшок з алюмініевай фальгі, 25 кг/кардонны барабан або ў адпаведнасці з патрабаваннямі заказчыка.
Умовы захоўвання:Трымайце кантэйнер шчыльна закрытым і захоўвайце ў прахалодным, сухім і добра вентыляваным складзе, удалечыні ад несумяшчальных рэчываў.Пазбягайце ўздзеяння прамых сонечных прамянёў, вільгаці і празмернага цяпла.
Дастаўка:Дастаўка па ўсім свеце паветраным транспартам FedEx / DHL Express.Забяспечце хуткую і надзейную дастаўку.


Коды рызыкі R21 - Шкодны пры кантакце са скурай
R36/38 - Пры пападанні ў вочы і скуру выклікае раздражненне.
R46 - Можа выклікаць спадчыннае генетычнае пашкоджанне
R62 - Магчымая рызыка парушэння фертыльнасці
R63 - Магчымая рызыка нанясення шкоды ненароджанаму дзіцяці
Апісанне бяспекі S25 - Пазбягайце кантакту з вачыма.
S26 - Пры трапленні ў вочы неадкладна прамыць вялікай колькасцю вады і звярнуцца па медыцынскую дапамогу.
S36/37 - Ужывайце адпаведнае ахоўнае адзенне і пальчаткі.
S53 - Пазбягаць ўздзеяння - перад ужываннем атрымаць спецыяльныя інструкцыі.
WGK Германія 3
RTECS HA3840000
Код ТН ЗЭД 2942000000
Гемцытабіну гідрахларыд (CAS: 122111-03-9) - гэта новы сінтэтычны дыфторнуклеазідны прэпарат, які з'яўляецца антыметабалічным і супрацьпухлінным.Ён даследаваны і распрацаваны кампаніяй Eli Lilly and Company і ў 1995 годзе быў ухвалены для ўключэння ў спісы Паўднёвай Афрыкі, Швецыі, Нідэрландаў, Аўстраліі і іншых краін. Упраўленне па кантролі за прадуктамі і лекамі ЗША (FDA) зацвердзіла яго ў якасці тэрапіі першай лініі для клінічнага лячэння немелкоклеточного рака лёгкіх і рака падстраўнікавай залозы.
У апошнія гады з'яўляюцца новыя прэпараты, такія як Гемцитабин, Паклитаксел, Доцетаксел, Виноребин - эфектыўныя прэпараты для лячэння немелкоклеточного рака лёгкіх (скарочана НМРЛ).У параўнанні з традыцыйнымі хіміятэрапеўтычнымі прэпаратамі гэтыя прэпараты валодаюць перавагамі высокага лячэбнага эфекту і нізкай таксічнасці.Гемцытабіну гідрахларыд - гэта новае пакаленне лекаў супраць метабалітаў і тып спецыяльнага лекі для клеткавага цыклу, які гуляе важную ролю ў фазе сінтэзу ДНК, а менавіта ў S-фазе клетак.Пры пэўных умовах гэта лекі можа прадухіляць прагрэсаванне клетак з фазы G1 у фазу S і валодае моцнай супрацьракавай актыўнасцю пры немелкоклеточном раку лёгкіх (НМРЛ).Замежныя даследаванні паказалі, што эфектыўнасць аднаразовага лячэння НМРЛ толькі гемцитабина гідрахларыдам складае каля 18% ~ 35%, у той час як камбінаванае лячэнне цисплатином эфектыўнасць НМРЛ складае 41,7%.Пры развітым НМРЛ эфектыўная хуткасць карбаплатыну складае 16%, што падобна на цысплатын, але мае нізкую таксічнасць, асабліва ў дачыненні да страўнікава-кішачных рэакцый, прыгнёту касцявога мозгу і таксічнай рэакцыі нырак і нервовых канчаткаў.У спалучэнні з карбаплатынам абодва яны валодаюць узаемнай каардынацыяй і дадатковым эфектам і могуць вырабляць больш высокі лячэбны эфект.
Гемцитабина гідрахларыд
C9H11F2N3O4·HCl 299,66
Цитидин, 2'-дезокси-2',2'-дифлуро-, моногидрохлорид.
2′-Дэзаксі-2′,2′-дыфторцытыдыну моногідрахларыд (β-ізамер) [122111-03-9].
»Гемцытабіну гідрахларыд змяшчае не менш за 97,5 працэнта і не больш за 101,5 працэнта C9H11F2N3O4·HCl, разлічаны на аснове "як ёсць".
[Асцярожна, гемцитабина гідрахларыд з'яўляецца моцным цытастатыкаў.Неабходна быць вельмі асцярожным, каб прадухіліць удыханне часціц і ўздзеянне на скуру.]
Упакоўка і захоўванне - захоўваць у герметычных кантэйнерах.
Маркіроўка. Калі ён прызначаны для падрыхтоўкі ін'екцыйных лекавых формаў, на этыкетцы пазначана, што ён стэрыльны або павінен быць падвергнуты дадатковай апрацоўцы падчас падрыхтоўкі ін'екцыйных лекавых формаў.
Даведачныя стандарты USP <11>-
USP Цытазін RS
USP Эндатаксін RS
USP гемцитабина гідрахларыд RS
Ідэнтыфікацыя-
A: Інфрачырвонае паглынанне <197K>.
B: Ён адпавядае патрабаванням тэстаў на хларыд <191>.
Удзельнае кручэнне <781S>: паміж +43 і +50, пры 20.
Доследны раствор: 10 мг на мл.
pH <791>: паміж 2,0 і 3,0, у растворы, які змяшчае 10 мг на мл.
Астатак пры гарэнні <281>: не больш за 0,1%.
Цяжкія металы, метад I <231>: 0,001%.
Храматаграфічная чысціня-
Рашэнне A- Працягвайце ў адпаведнасці з указаннямі для рухомай фазы аналізу.
Раствор B-Прыгатуйце адфільтраваны і дэгазаваны метанол.
Рухомая фаза - выкарыстоўвайце зменныя сумесі раствора A і раствора B, як указана ў храматаграфічнай сістэме.Пры неабходнасці ўнясіце карэктывы (гл. Прыдатнасць сістэмы ў раздзеле "Храматаграфія 621").
Рашэнне аб прыдатнасці сістэмы - Працягвайце, як указана ў аналізе.
Стандартны раствор - растварыце дакладна ўзважаную колькасць USP гемцытабіну гідрахларыду RS і USP Cytosine RS у вадзе і развядзіце колькасна і паэтапна, калі неабходна, каб атрымаць раствор з вядомай канцэнтрацыяй каля 2 мкг на мл кожнага.
Тэст-раствор - перанясіце каля 50 мг гемцытабіну гідрахларыду, дакладна ўзважыўшы, у 25-мл мерную колбу, растварыце і развядзіце вадой да патрэбнага аб'ёму і змяшайце.
Храматаграфічная сістэма (гл. храматаграфію 621) - працягвайце, як указана ў раздзеле "Аналіз".Храматограф запраграмаваны наступным чынам.
Час (хвіліны) Раствор A (%) Раствор B (%) Вымыванне
0–8 97 3 ізакратычны
8–13 97®50 3®50 лінейны градыент
13–20 50 50 ізакратычны
20–25 50®97 50®3 паўторнае ўраўнаважванне
Храматаграфуйце раствор для праверкі прыдатнасці сістэмы і запішыце пікавыя адказы ў адпаведнасці з указаннямі для працэдуры: адносны час утрымання складае каля 0,5 для анамера гемцытабіну і 1,0 для гемцытабіну;дазвол, R, паміж гемцитабин-анамерам і гемцитабином складае не менш за 8,0;і каэфіцыент хваста для гемцитабина не больш за 1,5.Храматаграфуйце стандартны раствор і запішыце пікавыя адказы ў адпаведнасці з указаннямі для працэдуры: адносны час утрымання складае каля 0,1 для цытазіну і 1,0 для гемцытабіну;адноснае стандартнае адхіленне для паўторных ін'екцый складае не больш за 2,0%.
Працэдура - Асобна ўвядзіце аб'ём (каля 20 мкл) стандартнага раствора і доследнага раствора ў храматограф, запішыце храматаграму і вымерайце ўсе пікавыя адказы.Разлічыце працэнтнае ўтрыманне цытазіну ва ўзятай долі гемцытабіна па формуле:
2,5 (Cc / W) (rt / rs)
у якім Cc - гэта канцэнтрацыя USP Cytosine RS у стандартным растворы, у мкг на мл;W - маса прынятага гемцытабіну ў мг;rt - пікавая рэакцыя на цытазін у доследным растворы;rs - рэакцыя на цытазін у стандартным растворы: выяўляецца не больш за 0,1% цытазіну.Разлічыце працэнт кожнай прымешкі, акрамя цытазіну, у долі гемцытабіну, узятай па формуле:
2,5 (Cs / W) (ri / rs)
у якім Cs - канцэнтрацыя USP гемцытабіну гідрахларыду RS у стандартным растворы, у мкг на мл;W - маса прынятага гемцытабіну ў мг;ri - пікавы водгук для кожнай прымешкі ў выпрабавальным растворы;rs - рэакцыя на гемцитабин ў стандартным растворы: выяўлена не больш за 0,1% гемцитабина -анамера або любой іншай асобнай прымешкі;а сума ўсіх прымешак не больш за 0,2%.Выключыце з сумы ўсіх прымешак любыя пікі, якія знаходзяцца ніжэй мяжы колькаснага вызначэння (0,02%).
Іншыя патрабаванні. Калі на этыкетцы пазначана, што гемцытабін гідрахларыд стэрыльны, ён адпавядае патрабаванням да бактэрыяльных эндатаксінаў і стэрыльнасці для гемцытабіну для ін'екцый.Калі на этыкетцы пазначана, што гемцытабіну гідрахларыд неабходна падвергнуць далейшай апрацоўцы падчас падрыхтоўкі ін'екцыйных лекавых формаў, гэта адпавядае патрабаванням да бактэрыяльных эндатаксінаў у Гемцытабіну для ін'екцый.
аналіз-
Рухомая фаза. Прыгатуйце адфільтраваны і дэгазаваны раствор, які змяшчае 13,8 г аднаасноўнага фасфату натрыю і 2,5 мл фосфарнай кіслаты ў 1000 мл вады.[заўвага - pH гэтага раствора знаходзіцца ў межах ад 2,4 да 2,6.]
Раствор для прыдатнасці сістэмы - Перанясіце каля 10 мг гемцытабіну гідрахларыду ў невялікі флакон, дадайце 4 мл раствора, які змяшчае 168 мг гідраксіду калію на мл метанолу, шчыльна зачыніце вечкам і апрацуйце ультрагукам.Награвайце пры 55°С ад 6 да 16 гадзін, дайце астыць і перанясіце змесціва ў 100-мл мерную колбу з паслядоўнымі прамываннямі 1% (аб'ём) фосфарнай кіслаты.Развядзіце 1% фосфарнай кіслатой да аб'ёму і змяшайце.[заўвага - гэты раствор змяшчае каля 0,02 мг на мл α-анамера гемцытабіну.]
Стандартная падрыхтоўка. Растворыце дакладна ўзважаную колькасць USP гемцытабіну гідрахларыду RS у вадзе і развядзіце колькасна і паэтапна, калі неабходна, вадой, каб атрымаць раствор з вядомай канцэнтрацыяй каля 0,1 мг на мл.
Падрыхтоўка да аналізу. Перанясіце прыкладна 20 мг гемцытабіну гідрахларыду, дакладна ўзважаныя, у 200-мл мерную колбу, растварыце і развядзіце вадой да патрэбнага аб'ёму і змяшайце.
Храматаграфічная сістэма (гл. Храматаграфія <621>) - вадкасны храматограф абсталяваны 275-нм дэтэктарам і калонкай 4,6 мм × 25 см, якая змяшчае 5-мкм ўпакоўку L7.Хуткасць патоку складае каля 1,2 мл у хвіліну.Правядзіце храматаграфію раствора для праверкі прыдатнасці сістэмы і запішыце пікавыя адказы ў адпаведнасці з указаннямі для працэдуры: раздзяленне, R, паміж анамерам гемцытабіну і гемцытабінам складае не менш за 8,0;і каэфіцыент хваста, вызначаны па гемцытабіну, не перавышае 1,5.Храматаграфуйце стандартны прэпарат і запішыце пікавыя адказы ў адпаведнасці з указаннямі для працэдуры: адноснае стандартнае адхіленне для паўторных ін'екцый складае не больш за 1,0%.
Працэдура - Асобна ўвядзіце роўныя аб'ёмы (каля 20 мкл) стандартнага прэпарата і аналізнага прэпарата ў храматограф, запішыце храматаграмы і вымерайце адказы для асноўных пікаў.Разлічыце колькасць, у мг, C9H11F2N3O4·HCl у долі гемцытабіну гідрахларыду па формуле:
200C(rU / rS)
у якой C - канцэнтрацыя, у мг на мл, USP гемцытабіну гідрахларыду RS у стандартным прэпараце;і rU і rS - пікавыя адказы, атрыманыя пры падрыхтоўцы аналізу і стандартнай падрыхтоўцы адпаведна.
-

Гемцытабін гідрахларыд CAS 122111-03-9 API U...
-

Гемцытабін CAS 95058-81-4 Аналіз 98,0~102,0%
-

Цефотиам гідрахларыд CAS 66309-69-1 API USP S...
-

Доксарубіцыну гідрахларыд CAS 25316-40-9 API ЗША...
-

Эналапрыл малеат CAS 76095-16-4 Аналіз 98,0~102...
-

Гуанфацын гідрахларыд Гуанфацын HCl CAS 291...
-

Иринотекана гідрахларыд CAS 100286-90-6 Чысціня...
-

Леветырацэтам LEV CAS 102767-28-2 API Factory U...
-

Налтрэксон гідрахларыд CAS 16676-29-2 API USP...
-

Носкапін гідрахларыд гідрат CAS 912-60-7 AP...
-

Левадопа (L-DOPA) CAS 59-92-7 99,0~100,5% USP B...
-

Дарунавір CAS 206361-99-1 Чысціня супраць ВІЧ ≥99,0...
-

Эзеціміб CAS 163222-33-1 Чысціня 98,5%~102,0% (...
-

Лазафаксіфен тартрат CAS 190791-29-8 Хіральны пу...
-

Бортезомиб CAS 179324-69-7 Чысціня ≥99,0% (ВЭЖХ)...
-

CAS 274901-16-5 Чысціня ≥99,0% (ВЭЖХ) API