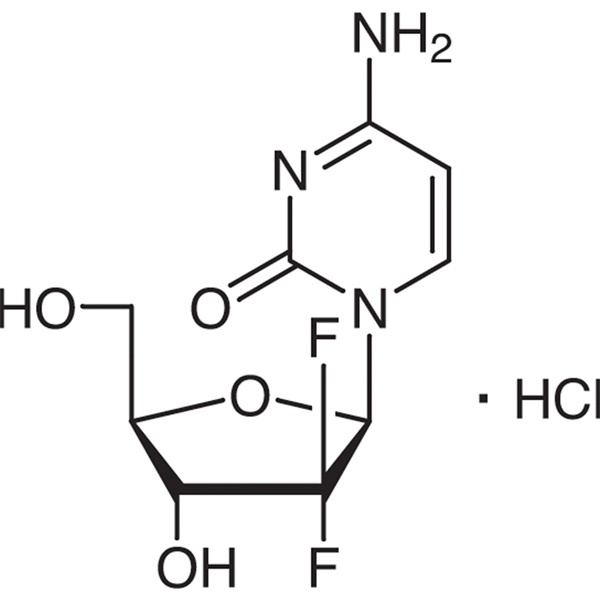
Gemcitabina klorhidrato CAS 122111-03-9 API USP35 estandarra
Ruifu Chemical Gemcitabine Hydrochloride (CAS: 122111-03-9) fabrikatzaile nagusia da, kalitate handiko ekoizpen komertziala duena.Ruifu Chemical-ek mundu osoko entrega, prezio lehiakorra, zerbitzu bikaina, kantitate txikiak eta ontziratuak eskaintzen ditu.Erosi Gemcitabine Hydrochloride,Please contact: alvin@ruifuchem.com
| Izen kimikoa | Gemcitabina klorhidratoa |
| Sinonimoak | Gemcitabina HCl;2'-desoxi-2',2'-difluorozitidina klorhidratoa;dFdC;dFdCyd;Gemzar;LY188011 klorhidratoa;Gemcitera;Gemsar |
| CAS zenbakia | 122111-03-9 |
| Erlazionatutako CAS | 95058-81-4 - Oinarri librea |
| Stock Egoera | Stock dago, Ekoizpen Ahalmena 5 Tona |
| Formula molekularra | C9H12ClF2N3O4 |
| Pisu Molekularra | 299,66 |
| Urtze-puntua | > 250 ℃ |
| Bidalketa Baldintza | Giro-tenperatura azpian |
| COA eta MSDS | Eskuragarri |
| Jatorria | Shanghai, Txina |
| Marka | Ruifu Kimika |
| Elementua | Zehaztapenak | Emaitzak |
| Itxura | Hauts kristalino zuria, usainik gabekoa | Betetzen du |
| Disolbagarritasuna | Uretan disolbagarria, metanolean apur bat disolbagarria, ia disolbaezina azetonan | Betetzen du |
| Identifikazioa IR | IR espektroak bat etorri behar du erreferentzia estandarrarena | Betetzen du |
| Identifikazioa Kloruroa | Positiboa.Klorurorako proben baldintzak betetzen ditu | Betetzen du |
| Irtenbidearen itxura | S soluzioa argi eta ez biziago erreferentziazko soluzioa baino koloreztatua BY7 | Betetzen du |
| pH | 2.0~3.0 | 2.6 |
| Errotazio espezifikoa [α]20/D | +43,0°-tik +50,0°-ra | +47,5° |
| Metal astunak (Pb) | ≤10ppm | <10 ppm |
| Lehortzean galtzea | ≤%1,00 | %0,3 |
| Piztean hondarrak | ≤0,10% | %0,03 |
| Lotutako substantziak | ||
| Zitosina | ≤0,10% | %0,01 |
| α-isomeroa | ≤0,10% | %0,01 |
| Beste edozein kutsadura | ≤0,10% | %0,04 |
| Ezpurutasun osoa | ≤%0,20 | %0,1 |
| Hondar-disolbatzaileak | ||
| Metanola | ≤%0,30 | Ez da detektatu |
| Toluenoa | ≤%0,01 | Ez da detektatu |
| Diklorometanoa | ≤%0,01 | Ez da detektatu |
| Azetona | ≤%0,50 | %0,1 |
| Saiakera | % 97,5 ~ % 101,5 (Oinarri lehorrean kalkulatua) | %99,9 |
| Ondorioa | USP35 Arauarekin bat dator | |
Paketea:Botila, aluminiozko paperezko poltsa, 25 kg / kartoizko danborra edo bezeroaren eskakizunaren arabera.
Biltegiratzeko egoera:Mantendu ontzia ondo itxita eta gorde biltegi fresko, lehor eta ondo aireztatutako substantzia bateraezinetatik urrun.Saihestu eguzki-argia, hezetasuna eta gehiegizko beroaren eraginpean egotea.
Bidalketa:Bidali mundu osora hegazkinez, FedEx / DHL Express bidez.Eman entrega azkarra eta fidagarria.


Arrisku-kodeak R21 - Kaltegarria azala ukitzean
R36/38 - Narritagarria begiak eta azala.
R46 - Herentziazko kalte genetikoak eragin ditzake
R62 - Ugalkortasuna urritzeko arriskua
R63 - Jaio gabeko umeari kalte egiteko arriskua
Segurtasunaren Deskribapena S25 - Saihestu begiekin kontaktua.
S26 - Begiekin kontaktuan egonez gero, garbitu berehala ur askorekin eta eskatu medikuari.
S36/37 - Erabili babes-arropa eta eskularru egokiak.
S53 - Saihestu esposizioa - eskuratu argibide bereziak erabili aurretik.
WGK Alemania 3
RTECS HA3840000
HS kodea 2942000000
Gemcitabine Hydrochloride (CAS: 122111-03-9) difluoro nukleosido sintetiko berri bat da, metaboliko eta antineoplasikoa dena.Eli Lilly and Company-k ikertu eta garatu du eta 1995ean Hegoafrikan, Suedian, Herbehereetan, Australian eta beste herrialde batzuetan zerrendatzea onartu zuen. Estatu Batuetako Elikagaien eta Droga Administrazioak (FDA) lehen lerroko terapia gisa onartu zuen. zelula ez-txikietako biriketako minbiziaren eta pankreako minbiziaren tratamendu klinikorako.
Azken urteotan, Gemcitabine, Paclitaxel, Docetaxel, Vinorebine bezalako sendagai berriak zelula ez-txikietako biriketako minbiziaren tratamendurako sendagai eraginkorrak dira (NSCLC laburtua).Kimioterapiako sendagai tradizionalekin alderatuta, sendagai hauek efektu sendagarri handiko eta toxikotasun baxuaren abantailak dituzte.Gemcitabine Hydrochloride metabolitoen aurkako sendagaien belaunaldi berri bat da eta zelulen ziklorako sendagai berezi mota bat da, DNAren sintesi fasean, hots, zelulen S fasean.Baldintza jakin batzuetan, sendagai honek zelulak G1 fasetik S fasera igarotzea ekidin dezake eta minbiziaren aurkako jarduera indartsua izan dezake zelula ez-zelula txikiko biriketako minbizia (NSCLC).Atzerriko ikerketek erakutsi dute Gemcitabine Hydrochloride-rekin NSCLC-ren tratamendu bakarraren eraginkortasuna % 18 ~ % 35 ingurukoa dela, cisplatinoarekin tratamendua konbinatuta NSCLCren eraginkortasuna % 41,7koa dela.NSCLC aurreratuan, karboplatinaren tasa eraginkorra % 16koa da, hau da, cisplatinoaren antzekoa, baina toxikotasun baxua du, batez ere erreakzio gastrointestinaletarako, hezur-muinaren zapalkuntzarako eta giltzurrun eta nerbio amaierako erreakzio toxikoetarako.Karboplatinarekin konbinatuta, biek elkarrekiko koordinazioa eta efektu gehigarria dute, eta efektu sendagarri handiagoak sor ditzakete.
Gemcitabina klorhidratoa
C9H11F2N3O4·HCl 299,66
Zitidina, 2′-desoxi-2′,2′-difluro-, monoklorhidratoa.
2′-Deoxi-2′,2′-difluorozitidina monoklorhidratoa (β-isomeroa) [122111-03-9].
»Gemcitabine Hydrochloride C9H11F2N3O4·HCl ehuneko 97,5 baino gutxiago eta ehuneko 101,5 baino gehiago ez dauka, den moduan kalkulatuta.
[Kontuz-Gemcitabine Hydrochloride agente zitotoxiko indartsua da.Kontuz ibili behar da partikulak arnastea eta larruazala berari ez erakusteko.]
Enbalatzea eta biltegiratzea-Kontserbatu ontzi estuetan.
Etiketatzea: dosi injektagarriak prestatzeko erabili nahi den tokian, etiketak antzua dela edo prozesatu gehiago egin behar duela dio dosi injektagarriak prestatzerakoan.
USP erreferentziako estandarrak <11>-
USP Zitosina RS
USP Endotoxina RS
USP Gemcitabine Hydrochloride RS
Identifikazioa-
A: infragorrien xurgapena <197K>.
B: Kloruroaren <191> proben baldintzak betetzen ditu.
Biraketa espezifikoa <781S>: +43 eta +50 artean, 20etan.
Proba disoluzioa: 10 mg ml bakoitzeko.
pH <791>: 2,0 eta 3,0 artean, ml bakoitzeko 10 mg dituen disoluzio batean.
<281> piztean hondarra: %0,1 baino gehiago ez.
Metal astunak, I metodoa <231>: % 0,001.
Garbitasun kromatografikoa-
A irtenbidea- Jarraitu Saiakuntzako fase mugikorrerako agindu bezala.
B disoluzioa-Prestatu metanola iragazi eta desgasifikatu.
Fase mugikorra - Erabili A eta B soluzioaren nahasketa aldakorrak Sistema Kromatografikoaren arabera zuzenduta.Egin doikuntzak, behar izanez gero (ikus Sistemaren egokitasuna Kromatografia 621 atalean).
Sistemaren egokitasunari buruzko irtenbidea- Jarraitu Saiakeran adierazitako moduan.
Disoluzio estandarra: disolbatu zehatz-mehatz pisatutako USP Gemcitabine Hydrochloride RS eta USP Cytosine RS uretan, eta kuantitatiboki diluitu, eta beharrezkoa bada urratsez urrats, bakoitzaren ml bakoitzeko 2 µg inguruko kontzentrazio ezaguna duen disoluzioa lortzeko.
Proba-disoluzioa: transferitu 50 mg inguru Gemcitabina klorhidrato, zehaztasunez pisatutakoa, 25 ml-ko matraz aforatu batera, disolbatu eta urarekin diluitu bolumenera eta nahastu.
Sistema kromatografikoa (ikusi Kromatografia 621)-Jarraitu Saiakuntzan agindu bezala.Kromatografoa honela programatzen da.
Denbora (minutuak) A disoluzioa (%) B disoluzioa (%) Eluzioa
0–8 97 3 isokratikoa
8–13 97®50 3®50 gradiente lineala
13–20 50 50 isokratikoa
20–25 50®97 50®3 berriro orekatzea
Sistemaren egokitasun-soluzioa kromatografiatu, eta erregistratu gailur-erantzunak Prozedurarako agindu bezala: atxikipen-denbora erlatiboak 0,5 ingurukoak dira gemcitabina -anomerorako eta 1,0 gemcitabinerako;gemcitabina -anomero eta gemcitabinaren arteko bereizmena, R, ez da 8,0 baino txikiagoa;eta gemcitabinaren isats-faktorea ez da 1,5 baino gehiago.Disoluzio estandarra kromatografiatu, eta erregistratu gailurreko erantzunak Prozedurarako agindu bezala: atxikipen-denbora erlatiboak 0,1 ingurukoak dira zitosinarentzat eta 1,0 gemcitabinarentzat;injekzio errepikatuen desbideratze estandar erlatiboa ez da % 2,0 baino handiagoa.
Prozedura: bereizita injektatu disoluzio estandarraren eta probako soluzioaren bolumen bat (20 µL inguru) kromatografoan, grabatu kromatograma eta neurtu gailur erantzun guztiak.Kalkulatu formula honen bidez hartutako gemcitabinaren zatian dagoen zitosinaren ehunekoa:
2,5 (Cc / W) (rt / rs)
zeinetan Cc USP Zitosina RS-ren kontzentrazioa disoluzio estandarrean, µg-tan mL bakoitzeko;W hartutako Gemcitabinaren pisua da, mgtan;rt Proba-disoluzioko zitosinaren erantzun gorena da;eta rs disoluzio estandarrean zitosinaren erantzuna da: ez da zitosinaren % 0,1 baino gehiago aurkitzen.Kalkulatu zitosina ez den ezpurutasun bakoitzaren ehunekoa formula honen bidez hartutako Gemcitabinaren zatian:
2,5(Cs/W)(ri/rs)
zeinetan Cs USP Gemcitabine Hydrochloride RS-ren kontzentrazioa disoluzio estandarrean, µg-tan ml bakoitzeko;W hartutako Gemcitabinaren pisua da, mgtan;ri Test disoluzioko ezpurutasun bakoitzaren erantzun gorena da;eta rs disoluzio estandarrean gemcitabinaren ondoriozko erantzuna da: gemcitabina -anomero edo beste edozein ezpurutasun indibidualaren % 0,1 baino gehiago ez da aurkitzen;eta ezpurutasun guztien batura ez da % 0,2 baino handiagoa.Ezpurutasun guztien baturatik kanpo kuantitazioaren mugatik behera dauden gailurrak (% 0,02).
Beste eskakizun batzuk-Etiketak Gemcitabine Hydrochloride antzua dela dioenean, bakterioen endotoxinak eta esterilitateak injekziorako Gemcitabineren azpian dauden baldintzak betetzen ditu.Etiketak dioenean Gemcitabine Hydrochloride prozesatu gehiago egin behar duela dosi injektagarriak prestatzen diren bitartean, Gemcitabine for Injekzioko endotoxina bakterianoen baldintzak betetzen ditu.
Saiakera-
Fase mugikorra: 1000 ml uretan 13,8 g sodio fosfato monobasiko eta 2,5 ml azido fosforiko dituen disoluzio iragazi eta desgasifikatu bat prestatu.[oharra- Disoluzio honen pHa 2,4 eta 2,6 artekoa da.]
Sistemaren egokitasunari buruzko irtenbidea - Transferitu 10 mg Gemcitabine Klorhidrato inguru ontzi txiki batera, gehitu 168 mg potasio hidroxido dituen disoluzio baten 4 ml metanol ml bakoitzeko, ondo itxi eta sonikatu.Berotu 55 tenperaturan 6 eta 16 orduz, utzi hozten eta edukia 100 ml-ko matraze bolumetriko batera transferitu azido fosforikoaren % 1 (v/v) ondoz ondoko garbiketarekin.Diluitu % 1eko azido fosforikoarekin bolumenean, eta nahastu.[Oharra - Soluzio honek gemcitabina α-anomero ml bakoitzeko 0,02 mg inguru ditu.]
Prestaketa estandarra - Uretan disolbatu USP Gemcitabine Hydrochloride RS zehaztasunez pisatutako kantitate bat, eta kuantitatiboki diluitu, eta beharrezkoa bada urratsez urrats, urarekin, ml bakoitzeko 0,1 mg inguruko kontzentrazio ezaguna duen disoluzioa lortzeko.
Entseguaren prestaketa-Transferitu 20 mg inguru Gemcitabina klorhidrato, zehaztasunez pisatutakoa, 200 ml-ko matraz aforatu batera, disolbatu eta urarekin diluitu bolumenera eta nahastu.
Sistema kromatografikoa (ikus Kromatografia <621>)-Kromatografo likidoa 275 nm-ko detektagailu bat eta 4,6 mm × 25 cm-ko zutabe batekin hornituta dago, 5 µm-ko L7 enbalamenduarekin.Emaria minutuko 1,2 ml ingurukoa da.Sistemaren egokitasun-soluzioa kromatografiatu, eta erregistratu gailur-erantzunak Prozedurarako agindu bezala: gemcitabina -anomeroaren eta gemcitabinaren arteko bereizmena, R, ez da 8,0 baino txikiagoa;eta gemcitabinatik zehazten den isats-faktorea ez da 1,5 baino handiagoa.Prestakuntza estandarra kromatografiatu eta erantzun gailurrak erregistratu Prozedurarako agindu bezala: injekzio errepikatuen desbideratze estandar erlatiboa ez da % 1,0 baino gehiagokoa.
Prozedura: bereizita injektatu estandarraren eta Entseguaren prestakinaren bolumen berdinak (20 µL inguru) kromatografoan, grabatu kromatogramak eta neurtu gailur nagusien erantzunak.Kalkulatu formula honen bidez hartutako gemcitabina klorhidratoaren zatian C9H11F2N3O4·HCl kantitatea, mgtan:
200C (rU / rS)
zeinetan C USP Gemcitabine Hydrochloride RS-ren kontzentrazioa, ml bakoitzeko mgtan, Prestaketa estandarrean;eta rU eta rS Assay prestaketatik eta Standard prestaketatik lortutako erantzun gailurrak dira, hurrenez hurren.
-

Gemcitabine Klorhidrato CAS 122111-03-9 API U...
-

Gemcitabine CAS 95058-81-4 Saiakera % 98,0 ~ 102,0
-

Cefotiam Klorhidrato CAS 66309-69-1 API USP S...
-

Doxorubicin Klorhidrato CAS 25316-40-9 API AEB...
-

Enalapril Maleate CAS 76095-16-4 Saiakera 98.0~102...
-

Guanfacine klorhidrato Guanfacine HCl CAS 291...
-

Irinotecan Hydrochloride CAS 100286-90-6 purutasuna...
-

Levetiracetam LEV CAS 102767-28-2 API Factory U...
-

Naltrexona klorhidrato CAS 16676-29-2 API USP...
-

Noscapine Klorhidrato Hidrato CAS 912-60-7 AP...
-

Levodopa (L-DOPA) CAS 59-92-7 99,0~100,5% USP B...
-

Darunavir CAS 206361-99-1 GIBaren aurkako purutasuna ≥99,0...
-

Ezetimibe CAS 163222-33-1 Garbitasuna % 98,5 ~ % 102,0 (...
-

Lasofoxifeno Tartrato CAS 190791-29-8 Pu Chiral...
-

Bortezomib CAS 179324-69-7 purutasuna ≥99,0% (HPLC)...
-

CAS 274901-16-5 Garbitasuna ≥99,0% (HPLC) API