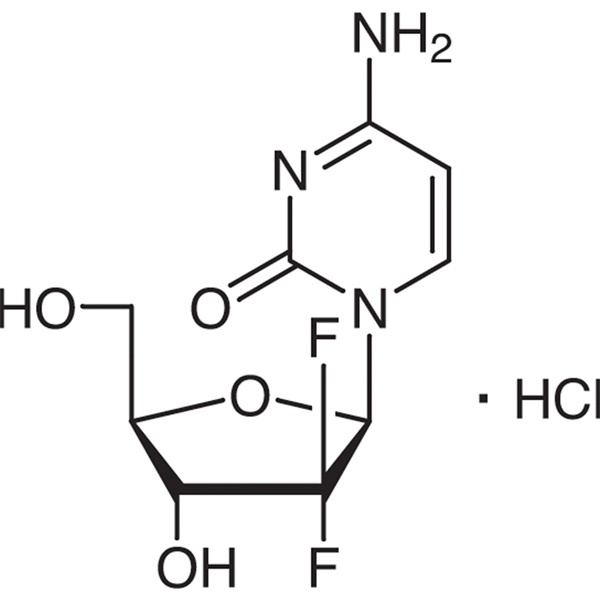
Clorhidrat de gemcitabină CAS 122111-03-9 Standard API USP35
Ruifu Chemical este cel mai mare producător de clorhidrat de gemcitabină (CAS: 122111-03-9) cu producție comercială de înaltă calitate.Ruifu Chemical poate oferi livrare în întreaga lume, preț competitiv, servicii excelente, cantități mici și vrac disponibile.Cumpărați clorhidrat de gemcitabină,Please contact: alvin@ruifuchem.com
| Nume chimic | Clorhidrat de gemcitabină |
| Sinonime | Gemcitabină HCI;Clorhidrat de 2'-deoxi-2',2'-difluorocitidină;dFdC;dFdCyd;Gemzar;LY188011 Clorhidrat;Gemcitera;Gemsar |
| Numar CAS | 122111-03-9 |
| CAS aferent | 95058-81-4 - Baza liberă |
| Starea stocului | În stoc, capacitate de producție 5 tone |
| Formulă moleculară | C9H12ClF2N3O4 |
| Greutate moleculară | 299,66 |
| Punct de topire | >250℃ |
| Condiție de livrare | Sub temperatura ambianta |
| COA și MSDS | Disponibil |
| Origine | Shanghai, China |
| Marca | Ruifu Chemical |
| Articol | Specificații | Rezultate |
| Aspect | Pulbere cristalină albă, fără miros | Se conformează |
| Solubilitate | Solubil în apă, ușor solubil în metanol, practic insolubil în acetonă | Se conformează |
| Identificare IR | Spectrul IR ar trebui să fie concordant cu cel al standardului de referinţă | Se conformează |
| Identificare Clorura | Pozitiv.Îndeplinește cerințele testelor pentru clorură | Se conformează |
| Aspectul soluției | Soluția S în clar și nu mai intens colorat decât soluția de referință BY7 | Se conformează |
| pH | 2,0~3,0 | 2.6 |
| Rotație specifică [a]20/D | +43,0° până la +50,0° | +47,5° |
| Metale grele (Pb) | ≤10 ppm | <10 ppm |
| Pierdere prin uscare | ≤1,00% | 0,3% |
| Rezidu la aprindere | ≤0,10% | 0,03% |
| Substante inrudite | ||
| Citozina | ≤0,10% | 0,01% |
| α-izomer | ≤0,10% | 0,01% |
| Orice altă impuritate | ≤0,10% | 0,04% |
| Impurități totale | ≤0,20% | 0,1% |
| Solventi reziduali | ||
| metanol | ≤0,30% | Nu a fost detectat |
| Toluen | ≤0,01% | Nu a fost detectat |
| Diclormetan | ≤0,01% | Nu a fost detectat |
| Acetonă | ≤0,50% | 0,1% |
| Test | 97,5%~101,5% (calculat pe bază uscată) | 99,9% |
| Concluzie | Conform standardului USP35 | |
Pachet:Sticlă, pungă din folie de aluminiu, 25 kg/tambur din carton sau conform cerințelor clientului.
Stare de depozitare:Păstrați recipientul bine închis și depozitați într-un depozit răcoros, uscat și bine ventilat, departe de substanțe incompatibile.Evitați expunerea la lumina directă a soarelui, umezeală și căldură excesivă.
Transport:Livrați în întreaga lume prin aer, prin FedEx / DHL Express.Oferiți livrare rapidă și fiabilă.


Coduri de risc R21 - Nociv în contact cu pielea
R36/38 - Iritant pentru ochi și piele.
R46 - Poate provoca leziuni genetice ereditare
R62 - Risc posibil de afectare a fertilităţii
R63 - Risc posibil de vătămare a fătului
Descrierea siguranței S25 - Evitați contactul cu ochii.
S26 - În caz de contact cu ochii, clătiți imediat cu multă apă și solicitați sfatul medicului.
S36/37 - Purtați îmbrăcăminte de protecție adecvată și mănuși.
S53 - Evitați expunerea - obțineți instrucțiuni speciale înainte de utilizare.
WGK Germania 3
RTECS HA3840000
Cod HS 2942000000
Clorhidratul de gemcitabină (CAS: 122111-03-9) este un nou medicament sintetic difluor nucleozidic care este antimetabolic și antineoplazic.Este cercetat și dezvoltat de Eli Lilly and Company și aprobat pentru a fi listat în Africa de Sud, Suedia, Țările de Jos, Australia și alte țări în 1995. Administrația Statelor Unite pentru Alimente și Medicamente (FDA) l-a aprobat ca terapie de primă linie pentru tratamentul clinic al cancerului pulmonar fără celule mici și al cancerului pancreatic.
În ultimii ani, medicamente noi precum Gemcitabină, Paclitaxel, Docetaxel, Vinorebine sunt medicamente eficiente pentru tratamentul cancerului pulmonar cu celule non-mici (abreviat NSCLC).În comparație cu medicamentele tradiționale de chimioterapie, aceste medicamente au avantajele unui efect curativ ridicat și toxicitate scăzută.Clorhidratul de gemcitabină este o nouă generație de medicamente anti-metaboliți și un tip de medicament special pentru ciclul celular, care joacă un rol major în faza de sinteză a ADN-ului, și anume faza S a celulelor.În anumite condiții, acest medicament poate preveni progresia celulelor de la faza G1 la faza S și are o activitate anticanceroasă puternică a cancerului pulmonar fără celule mici (NSCLC).Studiile străine au arătat că eficiența unui singur tratament pentru NSCLC cu clorhidrat de gemcitabină este de aproximativ 18% ~ 35%, în timp ce tratamentul combinat cu cisplatină eficiența pentru NSCLC este de 41,7%.În NSCLC avansat, rata eficientă a carboplatinei este de 16%, ceea ce este similar cu cisplatinei, dar are toxicitate scăzută, în special pentru reacțiile gastrointestinale, supresia măduvei osoase și reacția toxică a rinichilor și terminațiilor nervoase.În combinație cu carboplatina, ambele au un efect de coordonare și aditiv reciproc și pot produce efecte curative mai mari.
Clorhidrat de gemcitabină
C9H11F2N3O4.HCI 299,66
Citidină, 2′-deoxi-2′,2′-difluro-, monoclorhidrat.
Monoclorhidrat de 2′-deoxi-2′,2′-difluorocitidină (izomer p) [122111-03-9].
» Clorhidratul de gemcitabină conține nu mai puțin de 97,5 la sută și nu mai mult de 101,5 la sută C9H11F2N3O4·HCl, calculat pe baza de fapt.
[Atenție-Clorhidratul de gemcitabină este un agent citotoxic puternic.Trebuie avută mare grijă pentru a preveni inhalarea particulelor și expunerea pielii la acestea.]
Ambalare și depozitare-Conservați în recipiente etanșe.
Etichetare - Acolo unde este destinat utilizării la prepararea formelor de dozare injectabile, eticheta afirmă că este steril sau trebuie supus unei prelucrări ulterioare în timpul preparării formelor de dozare injectabile.
Standarde de referință USP <11>-
USP Citozină RS
USP Endotoxin RS
USP Clorhidrat de gemcitabină RS
Identificare-
A: Absorbție în infraroșu <197K>.
B: Îndeplinește cerințele testelor pentru clorură <191>.
Rotație specifică <781S>: între +43 și +50, la 20.
Soluție de testare: 10 mg per ml.
pH <791>: între 2,0 și 3,0, într-o soluție care conține 10 mg per ml.
Rezidu la aprindere <281>: nu mai mult de 0,1%.
Metale grele, Metoda I <231>: 0,001%.
Puritatea cromatografică-
Soluția A- Se procedează conform instrucțiunilor pentru faza mobilă din test.
Soluția B-Se prepară metanol filtrat și degazat.
Faza mobilă - Folosiți amestecuri variabile de Soluție A și Soluție B conform instrucțiunilor din sistemul cromatografic.Efectuați ajustări, dacă este necesar (consultați Adecvarea sistemului la Cromatografie 621).
Soluție de adecvare a sistemului - Procedați conform instrucțiunilor din Test.
Soluție standard - Se dizolvă o cantitate cântărită cu precizie de USP Gemcitabină Clorhidrat RS și USP Citozină RS în apă și se diluează cantitativ și treptat, dacă este necesar, pentru a obține o soluție cu o concentrație cunoscută de aproximativ 2 µg per ml din fiecare.
Soluție de testare - Se transferă aproximativ 50 mg de clorhidrat de gemcitabină, cântărite cu precizie, într-un balon cotat de 25 ml, se dizolvă și se diluează cu apă până la volum și se amestecă.
Sistem cromatografic (vezi Cromatografia 621) - Se procedează conform instrucțiunilor din Test.Cromatograful este programat după cum urmează.
Timp (minute) Soluție A (%) Soluție B (%) Eluare
0–8 97 3 izocratic
8–13 97®50 3®50 gradient liniar
13–20 50 50 izocratic
20–25 50®97 50®3 reechilibrare
Se cromatografiază soluția de adecvare a sistemului și se înregistrează răspunsurile de vârf conform indicațiilor pentru Procedură: timpii de retenție relativi sunt de aproximativ 0,5 pentru gemcitabină -anomer și 1,0 pentru gemcitabină;rezoluția, R, între gemcitabină -anomer și gemcitabină nu este mai mică de 8,0;iar factorul de decantare pentru gemcitabină nu este mai mare de 1,5.Se cromatografiază soluția standard și se înregistrează răspunsurile de vârf conform instrucțiunilor pentru Procedură: timpii relativi de retenție sunt de aproximativ 0,1 pentru citozină și 1,0 pentru gemcitabină;abaterea standard relativă pentru injecțiile repetate nu este mai mare de 2,0%.
Procedură - Injectați separat un volum (aproximativ 20 µL) de soluție standard și soluție de testare în cromatograf, înregistrați cromatograma și măsurați toate răspunsurile de vârf.Calculați procentul de citozină din porția de gemcitabină luată cu formula:
2,5(Cc/W)(rt/rs)
în care Cc este concentrația de USP Citozină RS în soluția standard, în µg per ml;W este greutatea, în mg, a Gemcitabinei luate;rt este răspunsul de vârf pentru citozină în soluția de testare;iar rs este răspunsul pentru citozină în soluția standard: nu se găsește mai mult de 0,1% din citozină.Calculați procentul fiecărei impurități, altele decât citozină, în porția de gemcitabină luată cu formula:
2,5(Cs/W)(ri/rs)
în care Cs este concentrația de clorhidrat de gemcitabină USP RS în soluția standard, în µg per ml;W este greutatea, în mg, a Gemcitabinei luate;ri este răspunsul de vârf pentru fiecare impuritate din soluția de testare;și rs este răspunsul datorat gemcitabinei în soluția standard: nu se găsește mai mult de 0,1% de gemcitabină -anomer sau orice altă impuritate individuală;iar suma tuturor impurităților nu este mai mare de 0,2%.Excludeți din suma tuturor impurităților orice vârfuri care sunt sub limita de cuantificare (0,02%).
Alte cerințe-Acolo unde eticheta afirmă că clorhidratul de gemcitabină este steril, acesta îndeplinește cerințele pentru endotoxine bacteriene și sterilitate sub gemcitabină pentru injecție.În cazul în care eticheta afirmă că clorhidratul de gemcitabină trebuie supus unei prelucrări ulterioare în timpul preparării formelor de dozare injectabilă, aceasta îndeplinește cerințele pentru Endotoxine bacteriene din Gemcitabină pentru injecție.
Test-
Faza mobilă - Se prepară o soluție filtrată și degazată care conține 13,8 g de fosfat de sodiu monobazic și 2,5 ml de acid fosforic în 1000 ml de apă.[notă- pH-ul acestei soluții este între 2,4 și 2,6.]
Soluție adecvată pentru sistem - Transferați aproximativ 10 mg de clorhidrat de gemcitabină într-un flacon mic, adăugați 4 ml dintr-o soluție care conține 168 mg de hidroxid de potasiu per ml de metanol, acoperiți strâns și sonicați.Se încălzește la 55°C timp de 6 până la 16 ore, se lasă să se răcească și se transferă conținutul într-un balon cotat de 100 ml cu spălări succesive cu acid fosforic 1% (v/v).Se diluează cu acid fosforic 1% până la volum și se amestecă.[notă-Această soluție conține aproximativ 0,02 mg per ml de gemcitabină α-anomer.]
Preparat standard - Se dizolvă o cantitate cântărită cu precizie de USP Gemcitabin Hydrochloride RS în apă și se diluează cantitativ, și treptat, dacă este necesar, cu apă pentru a obține o soluție cu o concentrație cunoscută de aproximativ 0,1 mg per ml.
Pregătirea testului - Se transferă aproximativ 20 mg de clorhidrat de gemcitabină, cântărite cu precizie, într-un balon cotat de 200 ml, se dizolvă și se diluează cu apă până la volum și se amestecă.
Sistem cromatografic (vezi Cromatografia <621>)-Cromatograful lichid este echipat cu un detector de 275 nm și o coloană de 4,6 mm × 25 cm care conține garnitura L7 de 5 µm.Debitul este de aproximativ 1,2 ml pe minut.Cromatografiați soluția de adecvare a sistemului și înregistrați răspunsurile de vârf conform indicațiilor pentru Procedură: rezoluția, R, între anomerul de gemcitabină și gemcitabină nu este mai mică de 8,0;iar factorul de decantare determinat din gemcitabină nu este mai mare de 1,5.Cromatografiați preparatul standard și înregistrați răspunsurile de vârf conform instrucțiunilor pentru Procedură: abaterea standard relativă pentru injecțiile repetate nu este mai mare de 1,0%.
Procedură - Se injectează separat volume egale (aproximativ 20 µL) de preparat standard și preparat de testare în cromatograf, înregistrați cromatogramele și măsurați răspunsurile pentru vârfurile majore.Calculați cantitatea, în mg, de C9H11F2N3O4·HCl în porția de clorhidrat de gemcitabină luată cu formula:
200C(rU / rS)
în care C este concentrația, în mg per ml, a clorhidratului de gemcitabină USP RS din preparatul standard;și rU și rS sunt răspunsurile de vârf obținute din preparatul de testare și, respectiv, din preparatul standard.
-

Clorhidrat de gemcitabină CAS 122111-03-9 API U...
-

Gemcitabină CAS 95058-81-4 Test 98,0~102,0%
-

Clorhidrat de Cefotiam CAS 66309-69-1 API USP S...
-

Clorhidrat de doxorubicină CAS 25316-40-9 API SUA...
-

Maleat de enalapril CAS 76095-16-4 Test 98,0~102...
-

Clorhidrat de guanfacină Guanfacină HCl CAS 291...
-

Clorhidrat de irinotecan CAS 100286-90-6 Puritate...
-

Levetiracetam LEV CAS 102767-28-2 API Factory U...
-

Clorhidrat de naltrexonă CAS 16676-29-2 API USP...
-

Clorhidrat de Noscapină Hidrat CAS 912-60-7 AP...
-

Levodopa (L-DOPA) CAS 59-92-7 99,0~100,5% USP B...
-

Darunavir CAS 206361-99-1 Puritate anti-HIV ≥99,0...
-

Ezetimibe CAS 163222-33-1 Puritate 98,5%~102,0% (...
-

Lasofoxifen Tartrat CAS 190791-29-8 Chiral Pu...
-

Bortezomib CAS 179324-69-7 Puritate ≥99,0% (HPLC)...
-

CAS 274901-16-5 Puritate ≥99,0% (HPLC) API