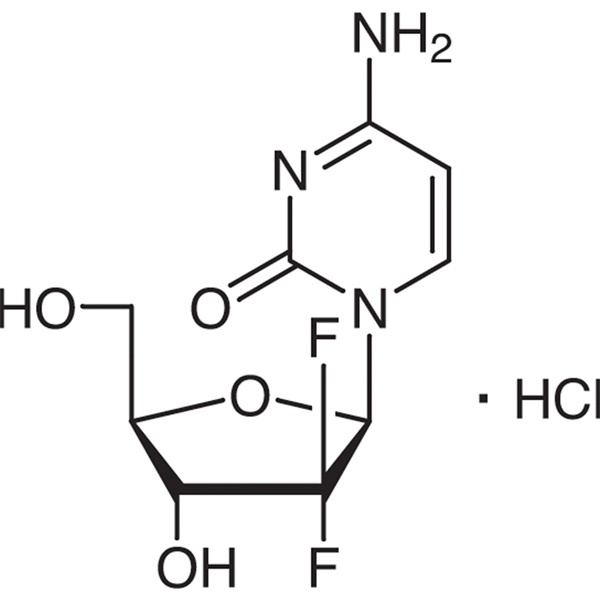
Gemcitabín hydrochlorid CAS 122111-03-9 API USP35 štandard
Ruifu Chemical je popredným výrobcom hydrochloridu gemcitabínu (CAS: 122111-03-9) s vysoko kvalitnou komerčnou výrobou.Ruifu Chemical môže poskytnúť celosvetovú dodávku, konkurencieschopnú cenu, vynikajúce služby, malé a veľké množstvá k dispozícii.Kúpiť gemcitabín hydrochlorid,Please contact: alvin@ruifuchem.com
| Chemický názov | Gemcitabín hydrochlorid |
| Synonymá | gemcitabín HCl;2'-deoxy-2',2'-difluórcytidín hydrochlorid;dFdC;dFdCyd;Gemzar;LY188011 hydrochlorid;Gemcitera;Gemsar |
| Číslo CAS | 122111-03-9 |
| Súvisiace CAS | 95058-81-4 - Voľná základňa |
| Stav skladu | Skladom, výrobná kapacita 5 ton |
| Molekulárny vzorec | C9H12CIF2N3O4 |
| Molekulová hmotnosť | 299,66 |
| Bod topenia | > 250 ℃ |
| Dodacia podmienka | Pod okolitou teplotou |
| COA a MSDS | K dispozícii |
| Pôvod | Šanghaj, Čína |
| Značka | Ruifu Chemical |
| Položka | technické údaje | Výsledky |
| Vzhľad | Biely kryštalický prášok, bez zápachu | Vyhovuje |
| Rozpustnosť | Rozpustný vo vode, mierne rozpustný v metanole, prakticky nerozpustný v acetóne | Vyhovuje |
| Identifikácia IR | IR spektrum by malo byť v súlade referenčného štandardu | Vyhovuje |
| Identifikačný chlorid | Pozitívny.Spĺňa požiadavky skúšok na chloridy | Vyhovuje |
| Vzhľad roztoku | Roztok S je číry a nie intenzívnejšie farebný ako referenčný roztok BY7 | Vyhovuje |
| pH | 2,0 až 3,0 | 2.6 |
| Špecifická rotácia [a]20/D | +43,0° až +50,0° | +47,5° |
| ťažké kovy (Pb) | ≤ 10 ppm | <10 str./min |
| Strata sušením | ≤ 1,00 % | 0,3 % |
| Zvyšok po zapálení | ≤ 0,10 % | 0,03 % |
| Súvisiace látky | ||
| Cytozín | ≤ 0,10 % | 0,01 % |
| a-Izomér | ≤ 0,10 % | 0,01 % |
| Akákoľvek iná nečistota | ≤ 0,10 % | 0,04 % |
| Celkové nečistoty | ≤ 0,20 % | 0,1 % |
| Reziduálne rozpúšťadlá | ||
| metanol | ≤ 0,30 % | Nezistený |
| toluén | ≤ 0,01 % | Nezistený |
| dichlórmetán | ≤ 0,01 % | Nezistený |
| Acetón | ≤ 0,50 % | 0,1 % |
| Skúška | 97,5 % ~ 101,5 % (vypočítané na sušenú bázu) | 99,9 % |
| Záver | Vyhovuje štandardu USP35 | |
Balíček:Fľaša, taška z hliníkovej fólie, 25 kg / kartónový bubon alebo podľa požiadavky zákazníka.
Stav skladovania:Nádobu uchovávajte tesne uzavretú a skladujte v chladnom, suchom a dobre vetranom sklade mimo dosahu nekompatibilných látok.Vyhnite sa priamemu slnečnému žiareniu, vlhkosti a nadmernému teplu.
Doprava:Doručujte do celého sveta letecky prostredníctvom FedEx / DHL Express.Poskytnite rýchle a spoľahlivé doručenie.


Rizikové kódy R21 - Škodlivý pri kontakte s pokožkou
R36/38 - Dráždi oči a pokožku.
R46 - Môže spôsobiť dedičné genetické poškodenie
R62 - Možné riziko poškodenia plodnosti
R63 - Možné riziko poškodenia nenarodeného dieťaťa
Popis bezpečnosti S25 - Zabráňte kontaktu s očami.
S26 - V prípade kontaktu s očami je potrebné ihneď ich vymyť s veľkým množstvom vody a vyhľadať lekársku pomoc.
S36/37 - Noste vhodný ochranný odev a rukavice.
S53 - Zabráňte expozícii - pred použitím sa oboznámte so špeciálnymi pokynmi.
WGK Nemecko 3
RTECS HA3840000
Kód HS 2942000000
Gemcitabín hydrochlorid (CAS: 122111-03-9) je syntetický nový difluórnukleozidový liek, ktorý je antimetabolický a antineoplastický.Je skúmaný a vyvinutý spoločnosťou Eli Lilly and Company a schválený na zaradenie do zoznamu v Juhoafrickej republike, Švédsku, Holandsku, Austrálii a ďalších krajinách v roku 1995. Americký Úrad pre kontrolu potravín a liečiv (FDA) ho schválil ako terapiu prvej línie. na klinickú liečbu nemalobunkového karcinómu pľúc a karcinómu pankreasu.
V posledných rokoch sú účinné lieky na liečbu nemalobunkového karcinómu pľúc (skrátene NSCLC) nové lieky ako Gemcitabín, Paclitaxel, Docetaxel, Vinorebine.V porovnaní s tradičnými chemoterapeutickými liekmi majú tieto lieky výhody vysokého liečebného účinku a nízkej toxicity.Gemcitabín hydrochlorid je nová generácia antimetabolitov a typ špeciálneho lieku pre bunkový cyklus, ktorý hrá hlavnú úlohu vo fáze syntézy DNA, konkrétne vo fáze S buniek.Za určitých podmienok môže tento liek zabrániť progresii buniek z fázy G1 do fázy S a má silnú protirakovinovú aktivitu, nemalobunkový karcinóm pľúc (NSCLC).Zahraničné štúdie ukázali, že účinnosť jedinej liečby NSCLC len s gemcitabín hydrochloridom je asi 18 % ~ 35 %, zatiaľ čo pri kombinovanej liečbe s cisplatinou je účinnosť pri NSCLC 41,7 %.Pri pokročilom NSCLC je účinná miera karboplatiny 16 %, čo je podobné ako cisplatina, ale má nízku toxicitu, najmä pre gastrointestinálne reakcie, supresiu kostnej drene a toxickú reakciu obličiek a nervových zakončení.V kombinácii s karboplatinou majú oba vzájomný koordinačný a aditívny účinok a môžu mať vyššie liečebné účinky.
Gemcitabín hydrochlorid
C9H11F2N304.HCl 299,66
Cytidín, 2'-deoxy-2',2'-difluór-monohydrochlorid.
2'-deoxy-2',2'-difluórcytidín monohydrochlorid (p-izomér) [122111-03-9].
»Gemcitabín hydrochlorid obsahuje nie menej ako 97,5 percent a nie viac ako 101,5 percent C9H11F2N3O4·HCl, vypočítané na základe stavu, v akom je.
[Pozor - Gemcitabín hydrochlorid je silná cytotoxická látka.Je potrebné venovať veľkú pozornosť tomu, aby ste zabránili vdýchnutiu častíc a vystaveniu pokožky.]
Balenie a skladovanie - Uchovávajte v tesných nádobách.
Označovanie - Ak je určený na použitie pri príprave injekčných dávkových foriem, na štítku sa uvádza, že je sterilný alebo sa musí podrobiť ďalšiemu spracovaniu počas prípravy injekčných dávkových foriem.
Referenčné štandardy USP <11>-
USP Cytosine RS
USP Endotoxín RS
USP Gemcitabine Hydrochloride RS
Identifikácia-
A: Infračervená absorpcia <197K>.
B: Spĺňa požiadavky testov na chlorid <191>.
Špecifická rotácia <781S>: medzi +43 a +50, pri 20.
Testovaný roztok: 10 mg na ml.
pH <791>: medzi 2,0 a 3,0 v roztoku obsahujúcom 10 mg na ml.
Zvyšok po zapálení <281>: nie viac ako 0,1 %.
Ťažké kovy, metóda I <231>: 0,001 %.
Chromatografická čistota -
Riešenie A – Postupujte podľa pokynov pre mobilnú fázu v teste.
Roztok B - Pripravte prefiltrovaný a odplynený metanol.
Mobilná fáza - Použite variabilné zmesi roztoku A a roztoku B podľa pokynov v chromatografickom systéme.V prípade potreby vykonajte úpravy (pozri Vhodnosť systému v časti Chromatografia 621).
Riešenie vhodnosti systému – Postupujte podľa pokynov v teste.
Štandardný roztok – presne odvážené množstvo USP Gemcitabine Hydrochloride RS a USP Cytosine RS rozpustite vo vode a zrieďte kvantitatívne av prípade potreby postupne, aby ste získali roztok so známou koncentráciou približne 2 ug na ml každého z nich.
Testovací roztok - Preneste približne 50 mg gemcitabín hydrochloridu, presne odváženého, do 25 ml odmernej banky, rozpustite vo vode a zrieďte vodou na požadovaný objem a premiešajte.
Chromatografický systém (pozri Chromatografiu 621) - Postupujte podľa pokynov v časti Skúška.Chromatograf je naprogramovaný nasledovne.
Čas (minúty) Roztok A (%) Roztok B (%) Elúcia
0–8 97 3 izokratické
8–13 97®50 3®50 lineárny gradient
13–20 50 50 izokratické
20–25 50®97 50®3 re-ekvilibrácia
Chromatografujte roztok vhodnosti pre systém a zaznamenajte maximálne odozvy podľa pokynov pre postup: relatívne retenčné časy sú približne 0,5 pre anomér gemcitabínu a 1,0 pre gemcitabín;rozlíšenie R medzi anomérom gemcitabínu a gemcitabínom nie je menšie ako 8,0;a chvostový faktor pre gemcitabín nie je väčší ako 1,5.Chromatografujte štandardný roztok a zaznamenajte maximálne odozvy podľa pokynov pre postup: relatívne retenčné časy sú približne 0,1 pre cytozín a 1,0 pre gemcitabín;relatívna štandardná odchýlka pre opakované injekcie nie je väčšia ako 2,0 %.
Postup – Oddelene vstreknite objem (asi 20 µl) štandardného roztoku a testovacieho roztoku do chromatografu, zaznamenajte chromatogram a zmerajte všetky maximálne odozvy.Vypočítajte percento cytozínu v časti gemcitabínu podľa vzorca:
2,5 (CC / W) (rt / rs)
v ktorom Cc je koncentrácia USP Cytosine RS v štandardnom roztoku v ug na ml;W je hmotnosť užitého gemcitabínu v mg;rt je maximálna odozva pre cytozín v testovacom roztoku;a rs je odpoveď pre cytozín v štandardnom roztoku: nenašlo sa viac ako 0,1 % cytozínu.Vypočítajte percento každej nečistoty inej ako cytozín v časti gemcitabínu podľa vzorca:
2,5 (Cs / W) (ri / rs)
v ktorom Cs je koncentrácia USP gemcitabín hydrochloridu RS v štandardnom roztoku v ug na ml;W je hmotnosť užitého gemcitabínu v mg;ri je maximálna odozva pre každú nečistotu v testovacom roztoku;a rs je odpoveď spôsobená gemcitabínom v štandardnom roztoku: nie je nájdených viac ako 0,1 % anoméru gemcitabínu alebo akejkoľvek inej jednotlivej nečistoty;a súčet všetkých nečistôt nie je väčší ako 0,2 %.Zo súčtu všetkých nečistôt vylúčte všetky píky, ktoré sú pod limitom kvantifikácie (0,02 %).
Ďalšie požiadavky – Ak je na etikete uvedené, že hydrochlorid gemcitabínu je sterilný, spĺňa požiadavky na bakteriálne endotoxíny a sterilitu podľa Gemcitabínu na injekciu.Ak sa na etikete uvádza, že hydrochlorid gemcitabínu sa musí podrobiť ďalšiemu spracovaniu počas prípravy injekčných liekových foriem, spĺňa požiadavky na bakteriálne endotoxíny podľa Gemcitabínu na injekciu.
Skúška-
Mobilná fáza - Pripravte prefiltrovaný a odplynený roztok obsahujúci 13,8 g dihydrogenfosforečnanu sodného a 2,5 ml kyseliny fosforečnej v 1000 ml vody.[poznámka - pH tohto roztoku je medzi 2,4 a 2,6.]
Roztok vhodnosti pre systém – Preneste približne 10 mg hydrochloridu gemcitabínu do malej liekovky, pridajte 4 ml roztoku obsahujúceho 168 mg hydroxidu draselného na ml metanolu, pevne uzavrite a sonikujte.Zahrievajte na 55 °C počas 6 až 16 hodín, nechajte vychladnúť a preneste obsah do 100 ml odmernej banky s postupným premytím 1 % (v/v) kyselinou fosforečnou.Zrieďte 1% kyselinou fosforečnou na objem a premiešajte.[Poznámka – Tento roztok obsahuje približne 0,02 mg na ml a-anoméru gemcitabínu.]
Štandardná príprava – Presne odvážené množstvo USP Gemcitabine Hydrochloride RS rozpustite vo vode a zrieďte kvantitatívne a v prípade potreby postupne vodou, aby ste získali roztok so známou koncentráciou približne 0,1 mg na ml.
Príprava testu - Preneste približne 20 mg hydrochloridu gemcitabínu, presne odváženého, do 200 ml odmernej banky, rozpustite a zrieďte vodou na požadovaný objem a premiešajte.
Chromatografický systém (pozri Chromatografia <621>) - Kvapalinový chromatograf je vybavený 275 nm detektorom a 4,6 mm x 25 cm kolónou, ktorá obsahuje 5 μm náplň L7.Prietok je približne 1,2 ml za minútu.Chromatografujte roztok vhodnosti pre systém a zaznamenajte maximálne odozvy podľa pokynov pre postup: rozlíšenie R medzi anomérom gemcitabínu a gemcitabínom nie je menšie ako 8,0;a chvostový faktor stanovený z gemcitabínu nie je väčší ako 1,5.Chromatografujte štandardný prípravok a zaznamenajte maximálne odozvy podľa pokynov pre postup: relatívna štandardná odchýlka pre replikované injekcie nie je väčšia ako 1,0 %.
Postup - Samostatne vstreknite rovnaké objemy (asi 20 µl) štandardného prípravku a prípravku testu do chromatografu, zaznamenajte chromatogramy a zmerajte odozvy pre hlavné píky.Vypočítajte množstvo C9H11F2N3O4·HCl v mg v časti hydrochloridu gemcitabínu podľa vzorca:
200C (rU / rS)
kde C je koncentrácia, v mg na ml, USP gemcitabín hydrochlorid RS v štandardnom prípravku;a rU a rS sú maximálne odozvy získané z prípravku testu a prípravku štandardu, v danom poradí.
-

Gemcitabín hydrochlorid CAS 122111-03-9 API U...
-

Gemcitabín CAS 95058-81-4 test 98,0 ~ 102,0 %
-

Cefotiam Hydrochloride CAS 66309-69-1 API USP S...
-

Doxorubicín hydrochlorid CAS 25316-40-9 API US...
-

Enalapril maleát CAS 76095-16-4 test 98,0~102...
-

Guanfacín hydrochlorid Guanfacín HCl CAS 291...
-

Irinotekan hydrochlorid CAS 100286-90-6 Čistota...
-

Levetiracetam LEV CAS 102767-28-2 API Factory U...
-

Naltrexón hydrochlorid CAS 16676-29-2 API USP...
-

Noskapín hydrochlorid hydrát CAS 912-60-7 AP...
-

Levodopa (L-DOPA) CAS 59-92-7 99,0~100,5% USP B...
-

Darunavir CAS 206361-99-1 Anti-HIV Čistota ≥99,0...
-

Ezetimib CAS 163222-33-1 Čistota 98,5 %~102,0 % (...
-

Lasofoxifén tartrát CAS 190791-29-8 Chiral Pu...
-

Bortezomib CAS 179324-69-7 Čistota ≥99,0 % (HPLC)...
-

CAS 274901-16-5 Čistota ≥99,0 % (HPLC) API